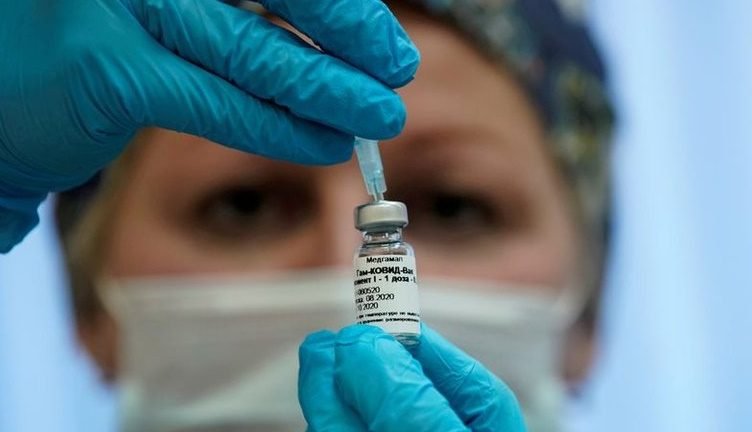
Sinopharm fue aplicada a 100 mil trabajadores de riesgo y también mostró resultados muy prometedores en México. Mientras que la vacuna Sputnik V tuvo un 92% de eficacia en las primeras pruebas de la fase tres según informó Gobierno Ruso.
Sinopharm
Frente a la crisis sanitaria mundial, varios laboratorios de distintos países compiten por hallar una vacuna contra el COVID-19. La Organización Mundial de la Salud (OMS) informó que existen 47 proyectos que son objeto de ensayos clínicos en humanos. Diez están en fase tres, la más avanzada, que implica a decenas de miles de voluntarios para probar su eficacia.
La farmacéutica estadounidense Pfizer y la empresa biotecnológica alemana BioNTechanunciaron una eficiencia del 90% según los primeros resultados de esa etapa.
Sinopharm, que también trabaja en la producción a escala de una vacuna, obtuvo datos muy alentadores. A diferencia de Pfizer, cuyos resultados surgen de ensayos clínicos, las conclusiones se basan en la observación después del uso de emergencia. “Aunque el primero tiene mayor autoridad académica, el segundo también es un estudio de control”, explicó el especialista Tao Lina al Global Times.
La fórmula fue desarrollada por China National Biotech Group, en colaboración con el Instituto de productos Biológicos de Beijing y la farmacéutica estatal china. Desde que comenzaron los estudios, fueron inoculadas 100 mil personas y hasta ahora ninguna ha presentado reacciones adversas. Entre ellos, hay 56 mil que realizaron viajes al exterior y ninguno contrajo el virus.
La mayoría de los voluntarios son empleados de China National Petroleum Corporation, China Petrochemical Corporotaion y de la tecnológica Huawei.
Sinopharm puntualizó sobre los resultados obtenidos en una oficina de México, donde 81 de 99 empleados se aplicaron la dosis. Ninguno de los inoculados contrajo el virus. En cambio, diez personas que no habían sido vacunadas protagonizaron un brote de coronavirus.
En agosto de este año, Liu Jingzhen, el presidente de la empresa estatal China National Biotec Group, parte de la farmacéutica Sinopharm, aseguró que la vacuna contra el coronavirus en la que trabaja el grupo estará lista “probablemente en diciembre” y tendrán la capacidad de producir más de mil millones de dosis en 2021.
Hasta ahora, China ha aprobado tres vacunas para uso urgente. Estos se han entregado a grupos de alto riesgo, como personal médico, diplomáticos enviados a los países más afectados y empleados enviados al extranjero bajo la Iniciativa Belt and Road.:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/PHQXFSVCDS4HNMVDMGDHIEVPXQ.jpg) En agosto de este año se dio a conocer que Liu Jingzhen, el presidente de la empresa estatal China National Biotec Group, parte de la farmacéutica Sinopharm, aseguró que la vacuna contra el coronavirus en la que trabaja el grupo estará lista “probablemente en diciembre” (REUTERS)
En agosto de este año se dio a conocer que Liu Jingzhen, el presidente de la empresa estatal China National Biotec Group, parte de la farmacéutica Sinopharm, aseguró que la vacuna contra el coronavirus en la que trabaja el grupo estará lista “probablemente en diciembre” (REUTERS)
El Ministerio de Ciencia y Tecnología de China informó a fines de octubre que más de 60.000 voluntarios recibieron alguna de las cuatro candidatas vacunas chinas contra el COVID19 “sin presentar efectos adversos significativos”. En ese marco, el laboratorioSinopharm comunicó que en su ensayo,realizado por el Instituto de Productos Biológicos de Pekín, hallaron “seguridad y tolerancia” a sus dosis en todos los grupos de edad, así como “inmunogenicidad”. Los investigadores publicaron los datos del estudio en la revista científica The Lancet y precisaron que el objetivo fue “evaluar la seguridad y tolerabilidad” de la vacuna inactivada BBIBP-CorV en pacientes de 60 años o más.
Desarrollada por el CNBG (China National Biotech Group en inglés), en colaboración con el BIBP (Instituto de productos Biológicos de Beijing) y la farmacéutica estatal china Sinopharm, BBIBP-CorV es una de las 10 vacunas que ya se prueban en humanos en Fase 3. El BIBP es un instituto precalificado por la OMS (Organización Mundial de la Salud), es el principal fabricante de vacunas de China y el único Instituto que cuenta con la aprobación regulatoria de Bioseguridad Nivel 3 para la fabricación de vacunas a base de cultivo de virus.
“Es una vacuna de virus inactivado, como es por ejemplo la de la hepatitis A, la de polio y la de la rabia, es decir vacunas que son absolutamente seguras desde ese punto de vista porque no contienen elementos de virus vivo”, precisó en diálogo con este medio el infectólogo argentino Pedro Cahn, director de Fundación Huésped y miembro del Comité Asesor del presidente Alberto Fernández en la lucha contra el nuevo coronavirus.
Por su parte, el infectólogo Eduardo López sostuvo que la vacuna de Sinopharm está basada en virus muerto. “Son virus que crecen en células Vero, que pertenecen a un linaje celular utilizado en cultivos celulares (el linaje Vero fue aislado a partir de las células epiteliales del riñón de un mono verde africano). Y luego de tener una cierta carga viral, la vacuna se inactiva a través de métodos químicos y luego se prepara para su aplicación. Esta plataforma ya se probó con éxito en la vacuna de la Hepatitis A, y para Polio”, recordó el especialista.:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/KPABGVVDB5HBFOSFUXV2SFXS3Y.jpg) La confianza en las vacunas de cosecha propia es clave para la diplomacia de salud pública de China frente a las acusaciones de Estados Unidos y otros países de que las demoras en los informes permitieron que el virus se propagara desde China (EFE/EPA/YFC/Archivo)
La confianza en las vacunas de cosecha propia es clave para la diplomacia de salud pública de China frente a las acusaciones de Estados Unidos y otros países de que las demoras en los informes permitieron que el virus se propagara desde China (EFE/EPA/YFC/Archivo)
China se encuentra entre los países que lideran la carrera mundial por una vacuna COVID-19, con cuatro tratamientos en las fases finales de los ensayos clínicos. Las autoridades sanitarias han dicho que una vacuna estará disponible en China a partir de noviembre o diciembre.
Bajo un programa de emergencia de vacunas que comenzó en julio, decenas de miles de voluntarios han recibido vacunas experimentales, lo que generó preguntas sobre los riesgos de administrar tratamientos no probados en el público.
En el marco del programa, China ofrece tres inyecciones experimentales desarrolladas por una unidad del gigante farmacéutico estatal China National Pharmaceutical Group y Sinovac Biotech, que cotiza en la bolsa estadounidense. Una cuarta vacuna que está desarrollando CanSino Biologics fue aprobada para su uso por el ejército chino en junio.
La confianza en las vacunas de cosecha propia es clave para la diplomacia de salud pública de China frente a las acusaciones de Estados Unidos y otros países de que las demoras en los informes permitieron que el virus se propagara desde China, convirtiéndose en una pandemia que se ha cobrado más de 1 millón de vidas.
Recientemente, China se unió a Covax, una iniciativa mundial de vacunas codirigida por la Organización Mundial de la Salud, Gavi, Vaccine Alliance y Coalition for Epidemic Preparedness and Innovations. Al unirse a la coalición, rechazada por Estados Unidos, China se convirtió en la mayor economía en participar.
Sputnik V
Rusia anunció que la vacuna Sputnik V alcanzó un 92% de efectividad en las primeras pruebas de la fase tres y que “no hubo eventos adversos inesperados durante los ensayos”.
El anuncio se produjo 48 horas después que la empresa farmacéutica estadounidense Pfizer confirmara que su vacuna logró un 90% de eficacia.
“La eficacia de la vacuna Sputnik V logró el 92% (cálculo basado en los 20 casos confirmados de COVID-19 divididos entre las personas vacunadas y las que recibieron el placebo). Actualmente, 40.000 voluntarios están participando en ensayos clínicos de fase III, doble ciego, aleatorizados y controlados con placebo, de los cuales más de 20.000 se han vacunado con la primera dosis de la vacuna y más de 16.000 tanto con la 1ª y 2ª dosis de la vacuna”, informaron el Centro Nacional Gamaleya de Epidemiología y Microbiología del Ministerio de Salud de la Federación de Rusia y el Fondo de Inversión Directa de Rusia (RDIF) a través de un comunicado de prensa.
“La eficacia se demostró sobre la base de un primer análisis intermedio obtenido 21 días después de la primera inyección. No hubo eventos adversos inesperados durante los ensayos. El seguimiento de los participantes está en curso”, añadieron.
“El primer registro mundial de la vacuna COVID-19, realizado en Rusia el 11 de agosto bajo el mecanismo de autorización de uso de emergencia, permite a la Federación de Rusia administrar la vacuna fuera de los ensayos clínicos a voluntarios como médicos y otros grupos de alto riesgo. Ensayos realizados con el uso civil de la vacuna en Rusia (que no forman parte de ensayos clínicos) basados en el seguimiento de 10.000 vacunados adicionales confirmaron la eficacia de la vacuna a una tasa superior al 90%”, señalaron las autoridades sanitarias rusas y el RDIF.:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/FL2DZUOCRJCCDIOCTMF3KUVPBM.jpg) Spuntik V, la primera vacuna rusa registrada contra la covid-19. EFE/EPA/SERGEI ILNITSKY/Archivo
Spuntik V, la primera vacuna rusa registrada contra la covid-19. EFE/EPA/SERGEI ILNITSKY/Archivo
El ministro de Salud de la Federación de Rusia, Mikhail Murashko, aseguró que “el uso de la vacuna y los resultados de los ensayos clínicos demuestran que es una solución eficaz para detener la propagación de la infección por coronavirus y una herramienta de atención médica preventiva». “Este es el camino más exitoso para derrotar la pandemia”, agregó.
Por su parte, el director del Centro Gamaleya, Alexander Gintsburg, afirmó que “la publicación de los resultados provisionales de los ensayos clínicos posteriores al registro que demuestran de manera convincente la eficacia de la vacuna Sputnik V da paso a la vacunación masiva en Rusia contra la enfermedad de COVID-19 en las próximas semanas”.
“Gracias al aumento de la producción en los nuevos sitios de fabricación, la vacuna Sputnik V pronto estará disponible para una población más amplia. Esto romperá la tendencia actual y conducirá a una eventual disminución de las tasas de infección por COVID-19, primero en Rusia y luego a nivel mundial”, añadió Gintsburg.
Mientras que Kirill Dmitriev, director ejecutivo de RDIF, señaló que “Sputnik V es la primera vacuna registrada contra COVID-19 en el mundo” y que se basa en una “plataforma segura y eficaz de vectores adenovirales humanos”. “Cada vez más países reconocen la plataforma de vectores adenovirales humanos y planean incluir estas vacunas, como las más estudiadas y conocidas, en sus respectivos portafolios nacionales de vacunas”, concluyó.:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/L44ZHRSCQMOGKFDI37JFSOII7Y.jpg) REUTERS/Tatyana Makeyeva/File Photo
REUTERS/Tatyana Makeyeva/File Photo
Según el comunicado, ya fueron solicitadas más de 1.200 millones de dosis de la vacuna Sputnik V provenientes de más de 50 países. Además, confirmaron que los suministros de vacunas para el mercado mundial serán producidos por los socios internacionales de RDIF en India, Brasil, China, Corea del Sur y otros países.
“Los contratos de RDIF existentes con socios internacionales permiten la producción anual de 500 millones de dosis de la vacuna Sputnik V fuera de Rusia. RDIF ahora está considerando solicitudes adicionales de varios países y empresas para aumentar aún más sus capacidades de producción en el extranjero”, indicó la nota de prensa.
Los datos de la investigación provisional serán publicados por el equipo del Centro Gamaleya en una de las principales revistas médicas internacionales. Tras la finalización de los ensayos clínicos de fase III de la vacuna Sputnik V, el Centro proporcionará acceso al informe completo del ensayo clínico, señaló el comunicado.
Actualmente, los ensayos clínicos de fase III del Sputnik V están aprobados y se están llevando a cabo en Bielorrusia, Emiratos Árabes Unidos, Venezuela y otros países, así como la fase II-III en India.
Fuente: Infobae